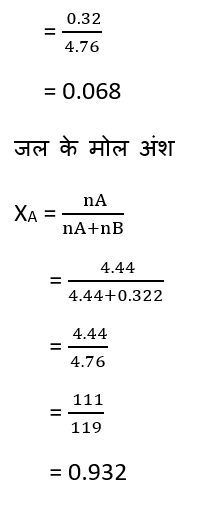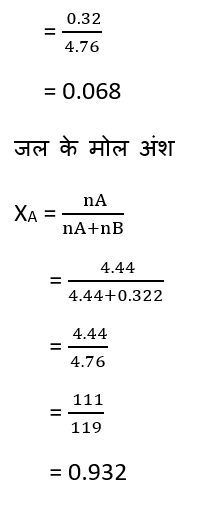Concentration of Solution.
सांद्रता – किसी विलयन के इकाई आयतन में उपस्थित विलेय पदार्थ की मात्रा को विलयन की सांद्रता कहते है.
विलयन की सांद्रता को निम्न पदों में व्यक्त किया जाता है.

Methods of measurement.
1. Mass percent (w/W)%

जैसे– 10 % (w/W)% ग्लूकोज का जल में विलयन का अर्थ है- 10 gm ग्लूकोज 90 gm जल में घोला गया है.
2 . Volume percent (V/v) %

जैसे– 10% (v/v)% एथेनॉल का जल में विलयन का अर्थ है- 10 ml एथेनॉल को 90 ml जल घुला गया है.
3. Mass-Volume Percentage (W/V) %

जैसे– फार्मेसी (दवाईयों में)
4 . Parts per million (PPM) – सांद्रता के इस पद का उपयोग उस स्थिति मे किया जाता है जब विलेय पदार्थ की मात्रा बहुत कम होती है।
जैसे– 1. पानी में घुली ऑक्सीजन
2 .पेय जल में घुलनशील लवणों की मात्रा

5. Mole Fraction – किसी विलयन मे किसी घटक/अवयव का मोलअंश उस घटक के मोलों की संख्या तथा विलयन में उपस्थित कुल मोलों की संख्या के अनुपात के बराबर होता है।
माना एक द्विअंगी विलयन में दो घटक A व B के मोलों की संख्या क्रमश: nA व nB है तथा इन घटको के मोलअंश क्रमश: XA व XB है. अतः घटक
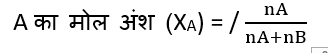
इसी प्रकार,\
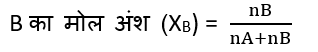
नोट– किसी विलयन में सभी घटकों के मोल अंश का योग 1 होता है.
6. Molarity – किसी विलयन के 1L आयतन में उपस्थित विलेग के मोलों की संख्या मोलरता कहलाती है।

Question – 10gm NaOH को 250ml जल में घोलकर विलयन बनाया गया है, मोलरता ज्ञात कीजिए ?

Question – उस विलयन की मोलरता की गणना करो जिसमें 5gm NaOH और 450ml विलयन में घुला हुआ है.
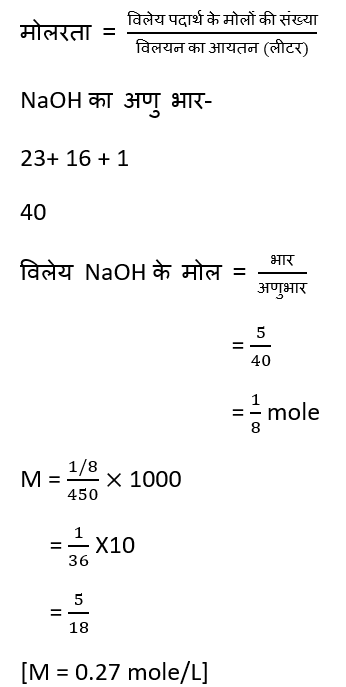
7. Molality (m) – विलायक के 1 kg द्रव्यमान में उपस्थित विलेय पदार्थ के मोलो की संख्या को मोललता कहते है। इसे m से प्रदर्शित करते है.
अथवा
1kg विलायक में घोले हुए विलेय के मोलो की संख्या को मोललता कहते है.
Question – 10gm यूरिया (NH2CONH2) को 500gm जल मे घोलकर विलयन बनाया गया है, विलयन की मोललता ज्ञात कीजिए ?
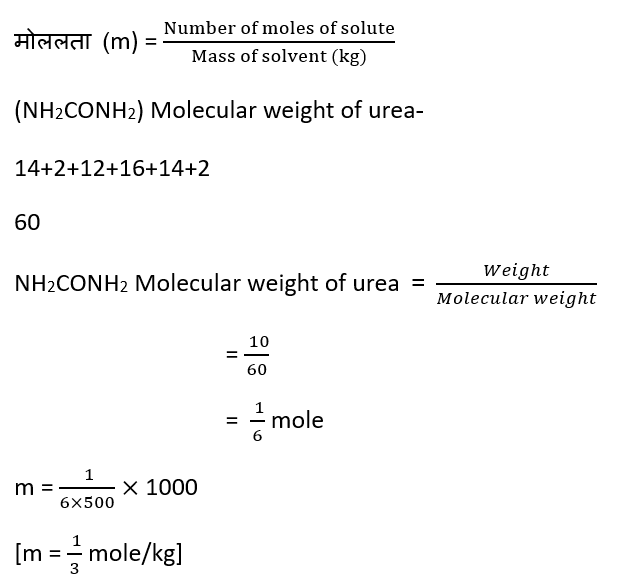
Question – 0.05mole एथेनॉइक अम्ल 250gm बेंजीन में घुलित विलयन है, विलयन की मोललता ज्ञात करो?

Question – मोललता व मोलरता में कौन विलयन की सांद्रता को अधिक यथार्थ (सही) रूप से प्रदर्शित करता है, क्यों?
Answer: मोललता में सांद्रता अधिक यथार्थता से प्रदर्शित की जाती है क्योंकि इस पर ताप का कोई प्रभाव नहीं होता।
नोट– द्रव्यमान प्रतिशत, मोलअंश, PPM, मोललता (m) तापमान पर निर्भर नहीं करते।
जबकि मोलरता (M), द्रव्यमान-आयतन प्रतिशत, आयतन-प्रतिशत तापमान पर निर्भर करते है.
Question – मोलरता की इकाई ?
Answer = Mole/L
Question – एथिलीन ग्लाइकॉल का 35% विलयन (V/v) वाहनों के इंजन को ठंडा करने में काम आता है, इसमें जल का आयतन ml में ज्ञात कीजिए ।
Answer: एथिलीन ग्लाइकॉल 35% (V/v) है। अतः यदि कुल आयतन 100 ml हो तो जल का आयतन
100-35 =65 ml होगा।
इसीलिए इस विलयन में जल का आयतन 65ml या 65% होगा।
Question – एथिलीन ग्लाइकॉल (C2H6O2) के मोल अंश की गणना करो, यदि विलयन में C2H6O2 का 20% द्रव्यमान उपस्थित हो?