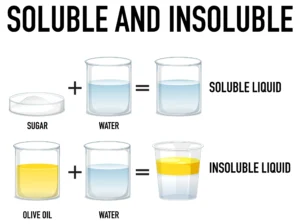
Osmosis and Osmotic Pressure.
अर्द्धपारगम्य झिल्ली द्वारा विलायक के अणुओ का कम सांद्र विलयन से अधिक सांद्र विलयन की ओर स्वतः प्रवाह परासरण कहलाता है।
- विलयन – उच्च सांद्रता विलयन – कम सांद्रता
- विलायक – निम्न सांद्रता विलायक- उच्च सांद्रता
Osmotic Pressure. किसी विलयन पर लगाया गया वह अतिरिक्त बाह्य दाब जो परासरण क्रिया को रोकता है, परासरण दाब कहलाता है।
अथवा
विलयन पर लगाया अतिरिक्त बाह्य दाब जो विलायक के अणु को निम्न सांद्रता वाले विलयन से उच्च सांद्रता वाले विलयन की ओर प्रवाह को रोक देता है।
विलायक के परासरण के कारण थिसेल फनल में विलयन का स्तर बढ जाता है।
नोट– यह प्रवाह दोनों विलयनो मे साम्य स्थापित होने तक सतत् बना रहता है।
ऐसी झिल्ली जिनसे होकर विलायक के अणु जा सकते है पर विलेय के अणु नहीं जा सकते,अर्द्धपारगम्य झिल्ली कहलाती है।
परासरण द्वारा उत्पन्न दाब , परासरण दाब कहलाता है।
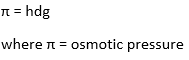
h = विलयन के स्तम्भ की उचाई
d = विलयन का घनत्व
g = गुरुत्व त्वरण
परासरण को रोकने के लिए परासरण दाब के तुल्य/बराबर अतिरिक्त दाब विलयन पर प्रयुक्त करना चाहिए ।
Description.
1.सर्वप्रथम एक आयताकार पात्र लेते है, यह पात्र दो समान भागों में अर्द्धपारगम्य झिल्ली (SPM) द्वारा पृथक होता है।
2.दोनो पात्र में पिस्टन P1 व P2 लगे है, पात्र के दोनों भागो A व B को क्रमशः शुद्ध विलायक एवं विलयन से भरते है।
3.परासरण के कारण शुद्ध विलायक के अणु विलयन की ओर गमन करते है। जिससे पिस्टन P2 ऊपर की ओर उठने लगता है व P1 नीचे की ओर जाता है।
4.अब पिस्टन P2 को प्रारंभिक अवस्था में लाने व साम्य अवस्था स्थापित करने के लिए बाह्य दाब प्रयुक्त करते है। यह बाह्य दाब परासरण को रोकने के लिए आवयश्यक है , अर्थात पिस्टन पर लगाया गया वह अतिरिक्त बाह्य दाब जिससे विलायक के अणु अर्द्धपारगम्य झिल्ली में से गमन नहीं कर पाते , परासरण दाब कहलाता है।
The osmotic pressure of a solution depends on the following factors .

नोट– वृहद अणुओ, बहुलको आदि का मोलर द्रव्यमान ज्ञात करने के लिए परासरण दाब अणुसंख्यक गुण का प्रयोग किया जाता है।
इसके निम्न कारण है-
1. परासरण दाब का मापन कमरे के ताप पर किया जा सकता है।
2. परासरण दाब का परिमाण अन्य अणुसंख्यक गुणों की तुलना में अधिक होता है।
3. परासरण दाब में सांद्रता मोलरता (M) के स्थान पर मोललता (m) में व्यक्त किया जाता है।
Examples of osmosis.
1. मुरझाए फूल तथा गाजर को पानी में रखने पर फूल जाता है।
2. कच्चे आमो का आचार डालने के लिए नमकीन जल में भिगोने पर वे संकुचित हो जाते है।
3. नमकीन जल में रखने पर रुधिर कोशिकाए सिकुड़ जाती है।
Q. कच्चे आम को सांद्र लवणीय विलयन में रखने पर क्या होता है ?
Ans.सांद्र लवणीय विलियन मे रखने पर बाह्य परासरण / बहिः परासरण के कारण जल को बाहर निकाल देता है एवं संकुचित हो जाता है।
परासरण दाब के आधार पर विलयनों के प्रकार – तीन प्रकार
1. समपरासरी विलयन (Isotonic)
2. अल्पपरासरी विलयन (hypotonic)
3. अतिपरासरी विलयन (hypertonic)
1. Isotonic Solution.
ऐसे दो विलयन जिनकी सांद्रता तथा परासरण दाब दिए गए ताप पर समान होते है, समपरासरी विलयन कहलाते है।
अथवा
दिए गए ताप पर सामान परासरण दाब वाले दो विलयन समपरासरी विलयन कहलाते है।
जब ऐसे विलयन अर्द्धपारगम्य झिल्ली द्वारा पृथक किये जाते है तो उनके बीच परासरण नहीं होता।
उदहारण- लाल रक्त कोशिकाओं में उपस्थित विलयन की सांद्रता 0.9 % (W/V) NaCl होती है ,जो एक समपरासरी विलयन है।
2. Hypotonic Solution
यदि दो विलयनों का परासरण दाब असमान हो तो कम परासरण दाब वाला विलयन अल्पपरासरी विलयन कहलाता है।
उदहारण – यदि लवण की सांद्रता 0.9 % (W/V) से कम हो तो जल कोशिका के अंदर प्रवाहित होगा और वे फूल जाएगी।
3. Hypertonic Solution
यदि दो विलयनों के परासरण दाब असमान हो तो अधिक परासरण दाब वाला विलयन, अतिपरासरी विलयन कहलाता है।
उदा.- यदि रक्त कोशिकाओं को 0.9 % (W/V) से अधिक NaCl विलयन मे रख दे तो जल कोशिका से बाहर प्रवाहित हो जाएगा और वे संकुचित हो जाएगी।
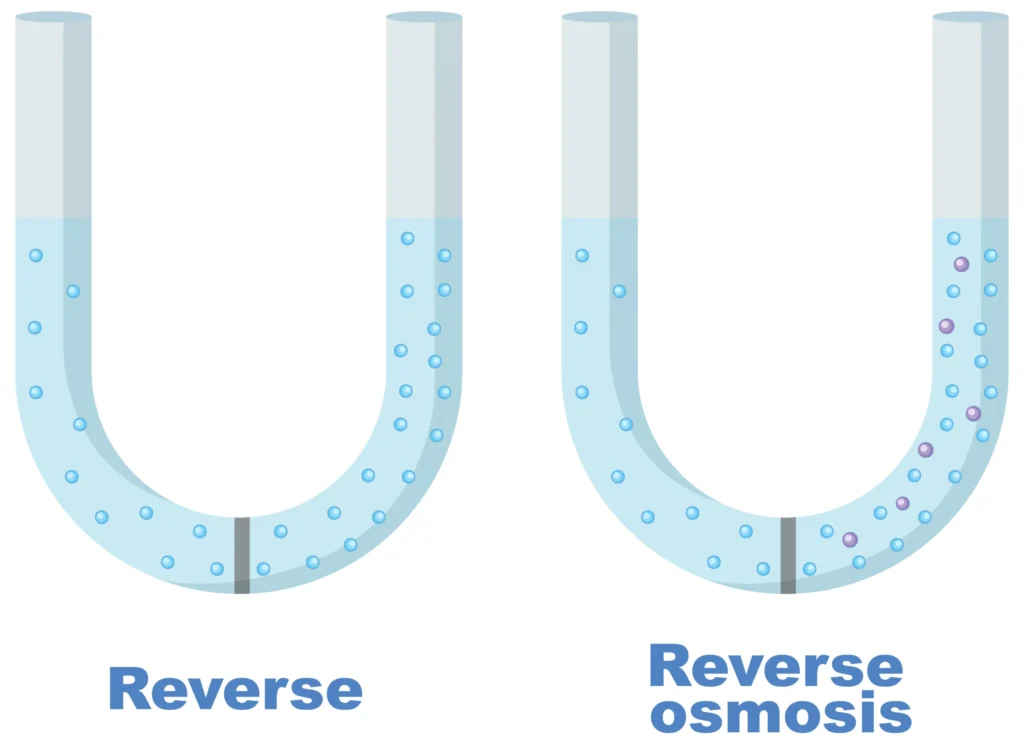
Reverse Osmosis.
जब विलयन पर परासरण दाब से अधिक दाब लगाया जाता है तो प्रतिलोम परासरण होता है।
Reverse Osmosis– किसी विलयन पर परासरण दाब से अधिक बाह्य दाब लगाने पर परासरण की क्रिया विपरीत दिशा में होने लगती है अर्थात विलायक के अणु अधिक सांद्रता वाले विलयन से कम सांद्रता वाले विलायक की ओर अर्द्धपारगम्य झिल्ली द्वारा गमन करते है। यह क्रिया प्रतिलोम परासरण (RO) कहलाती है।
Applications.
1. प्रतिलोम परासरण का उपयोग समुद्री जल के विलवणीकरण में किया जाता है।
2. R.O. उपकरण द्वारा जल को पीने योग्य बनाया जाता है।
नोट – प्रतिलोम परासरण में अर्द्धपारगम्य झिल्ली सेलूलोस ऐसीटेट की बनी होती है।
Q. प्रयोगशाला में सर्वाधिक प्रयुक्त होने वाली अर्द्धपारगम्य झिल्ली का नाम बताइए, यह कैसे बनाई जाती है?
उ. यह कॉपर फेरोसाइनाइड को Cu2 [ Fe (CN)6 ] है। इसे CuSO4 एवं K4 [Fe (CN)6 ] के सममोलर जलीय विलयनों को मिलाकर बनाया जाता है।