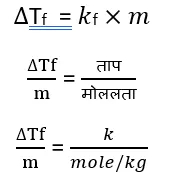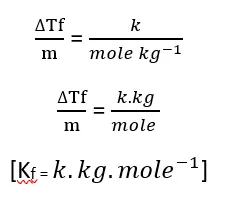Colligative Properties and the Calculation of Molecular Mass in Hindi.
ऐसे गुण जो किसी विलयन में विलेय पदार्थ की मात्रा अथवा अणुओ की संख्या पर निर्भर करते है, उसकी प्रकृति पर नहीं, अणु संख्यक गुणधर्म कहलाते है।
अणु संख्यक गुणधर्म चार प्रकार के होते है –
- वाष्पदाब में आपेक्षिक अवनमन
- क्वथनांक में उन्नयन
- हिमांक में अवनमन
- परसराण दाब
1. Relative Lowering of Vapor Pressure– किसी शुद्ध विलायक में अवाष्पशील विलेय पदार्थ मिलाने पर प्राप्त विलयन का वाष्पदाब शुद्ध विलायक की तुलना में हमेशा कम होता है। जिसे वाष्पदाब में अवनमन कहते है। अवाष्पशील विलेययुक्त विलयन का कुल वाष्पदाब केवल विलायक के कारण होता है।
माना विलायक का विलयन में वाष्पदाब P1 व मोलअंश X1 है एवं शुद्ध विलायक का वाष्पदाब P1° है अतः रॉउलट के नियम से ,

वाष्पदाब में अवनमन-
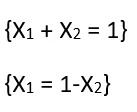

किसी विलयन की वाष्पदाब में आपेक्षिक अवनमन विलयन में उपस्थित मोलअंश के बराबर होता है।
समीकरण (2) से,
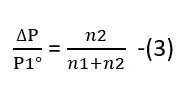
माना विलायक का द्रव्यमान W1 व मोलर द्रव्यमान M1 एवं विलेय का द्रव्यमान W2 व मोलर द्रव्यमान M2 है तो
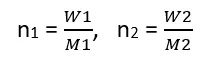
समीकरण (3) में मान रखने पर,
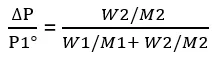
अतितनु विलयन के लिए W1/M1 >>> W2/M2 होता है। अतः W2/M2 को नगण्य मानने पर
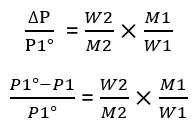
2. Elevation in Boiling Point-
क्वथनांक– किसी द्रव का क्वथनांक वह ताप होता है, जिस पर उस द्रव का वाष्पदाब वायुमंडलीय दाब के बराबर हो जाता है।
क्वथनांक में उन्नयन -किसी शुद्ध विलायक में कोई ठोस विलेय पदार्थ मिलाने पर प्राप्त विलयन का क्वथनांक शुद्ध विलायक के क्वथनांक से बढ़ जाता है।
अथवा
यदि किसी विलायक में अवाष्पशील विलेय की कुछ मात्रा मिला दी जाए तो विलयन का क्वथनांक विलायक से अधिक हो जाता है।
स्पष्टीकरण :- विलयन का वाष्पदाब शुद्ध विलायक की तुलना में कम होता है। विलयन के वाष्पदाब को वायुमंडलीय दाब के बराबर लाने के लिए विलायक की तुलना में अधिक ताप पर गर्म करना होता है, अतः विलयन का क्वथनांक शुद्ध विलायक से अधिक होता हैं.
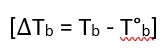
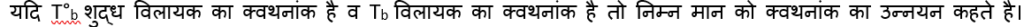
प्रयोगों के आधार पर यह निष्कर्ष निकाला गया कि तनु विलयनों के लिए क्वथनांक में उन्नयन विलयन की मोललता (m) के समानुपाती होता है।
अर्थात्
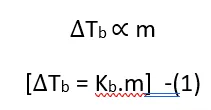
जहाँ kb = क्वथनांक में उन्नयन स्थिरांक
माना विलायक का द्रव्यमान W1 gm तथा विलेय का द्रव्यमान W2 gm एवं मोलर द्रव्यमान M2 है तो –

m का मान समीकरण 1 में रखने पर,

यदि M2 मोलर द्रव्यमान वाले विलेय के W2 gm, W1 gm विलायक में उपस्थित हो तो, विलयन की मोललता
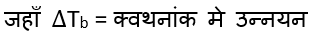
M2 = मोलर द्रव्यमान
3. Depression in Freezing Point
हिमांक– किसी द्रव का हिमांक वह ताप है जिस पर उस द्रव की वाष्प उसकी ठोस प्रावस्था के वाष्प के बराबर होती है।
हिमांक बिंदु पर द्रव तथा ठोस प्रावस्था परस्पर साम्यावस्था पर होती है।
हिमांक में अवनमन– किसी शुद्ध विलायक में ठोस विलेय पदार्थ मिलाने पर प्राप्त विलयन का हिमांक शुद्ध विलायक की तुलना में कम होता है, जिसे हिमांक में अवनमन कहते है।
अथवा
यदि किसी विलायक, अवाष्पशील विलेय की कुछ मात्रा मिला दी जाती है तो विलयन का हिमांक विलायक के हिमांक से कम हो जाता है। हिमांक में यह अवनमन एक अनुसंख्यक गुण है जो विलयन में विलेय के कणों की संख्या पर निर्भर करता है।
कारण– विलयन का वाष्पदाब शुद्ध विलायक के वाष्पदाब से कम होता है, अतः विलयन की द्रव अवस्था/प्रावस्था में वाष्पदाब उसकी ठोस प्रावस्था के वाष्पदाब के बराबर कम ताप पर ही प्राप्त होता है। अतः विलयन का हिमांक विलायक से कम होता है.
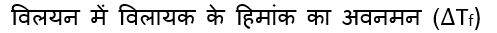
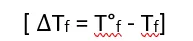
प्रयोगों के आधार पर यह निष्कर्ष निकाला गया कि तनु विलयनों हिमांक मे अवनमन विलयन की मोललता (m) के समानुपाती होता है।
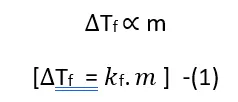
माना विलायक का द्रव्यमान W1 gm है तथा विलेय का द्रव्यमान W2 gm है तथा मोलर द्रव्यमान M2 है तो –

m का मान समीकरण 1 में रखने पर,
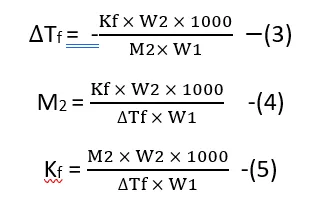
क्वथनांक उन्नयन स्थिरांक अथवा हिमांक अवनमन स्थिरांक की इकाई.