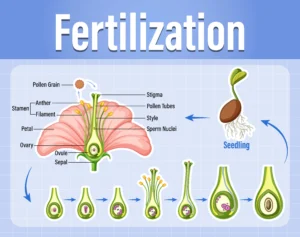
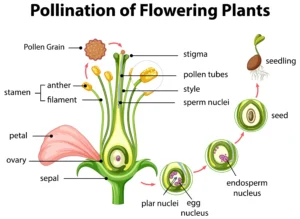
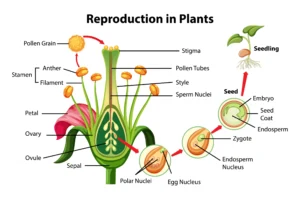
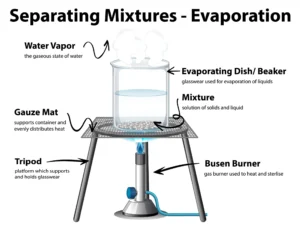
Vapor Pressure of Liquid Solutions in Hindi.
किसी वाष्पशील द्रव के द्वारा साम्यावस्था पर द्रव के वाष्प के द्वारा द्रव की सतह पर लगाया गया दाब उस सतह द्वारा द्रव पर वाष्पदाब कहलाता है.
- द्रव – वाष्पीकरण – वाष्प
- द्रव – संघनन – वाष्प

Liquid-Liquid Solution– किसी वाष्पशील विलायक में कोई वाष्पशील विलेय (द्रव) मिलाने पर प्राप्त विलयन में विलयन का वाष्प दाब दोनों घटको के वाष्पदाब के कारण होता है.
→ राउल्ट ने किसी वाष्पशील विलयन के लिए प्रत्येक घटक के आंशिक दाब तथा उस घटक के मोल अंश के मध्य मात्रात्मक संबंध दिया, जिसे राउल्ट का नियम कहते है.
OR
→ जब विलेय और विलायक दोनों द्रव होते है तो दोनों का वाष्पन होता है अर्थात् वाष्प बनती है, विलयन का कुल वाष्पदाब दोनों द्रवों के आंशिक वाष्पदाब के योग के बराबर होता है।
Raoult/Raoul’s Law.
इस नियम के अनुसार- एक विलयन में उपस्थित किसी वाष्पशील घटक का वाष्पदाब उसकी मोलभिन्न/मोल अंश के समानुपाती होता है।
माना किसी विलयन में वाष्पशील घटक 1 का वाष्पदाब P1 एवं विलयन मे उसका मोल अंश X1 है । उसी प्रकार, घटक 2 का आंशिक वाष्पदाब P2 व विलयन में उसका मोल अंश X2 है।
राउल्ट के नियमानुसार,
घटक 1 के लिए,
P1 X1
P1 = P1° X1 -(i)
जहाँ P1° = घटक 1 का शुद्ध अवस्था में वाष्पदाब
घटक 2 के लिए,
P2 X2
P2 = P2° X2 -(ii)
विलयन का कुल वाष्पदाब –
X1+X2=1
X1= 1-X2
P (Total) = P1 + P2
= P1° X1 + P2° X2
= P1° (1-X2) + P2° X2
= P1° -P1° X2 +P2° X2
= P1° +P2° X2 -P1° X2
[P = P1° + X2 (P2°-P1°)] -(iii)
→ निष्कर्ष :- समी. (iii) से निम्न निष्कर्ष निकाला जा सकता है.
1. विलयन का कुल वाष्पदाब घटक 1 व घटक 2 दोनों के मोल अंश से संबंधित किया जा है.
2. विलयन का कुल वाष्पदाब घटक 2 के मोल अंश X2 के साथ रेखीय संबंध दर्शाता है.
Graphical representation of Raoult’s law.
Solid-liquid solutions and vapor pressure.
किसी अवाष्पशील ठोस को द्रव विलायक में घोलने पर प्राप्त विलयन का वाष्पदाब शुद्ध विलायक की तुलना में हमेशा कम होता है, इसे वाष्पदाब का अवनमन कहते है।
किसी वाष्पशील द्रव विलायक में अवाष्पशील ठोस के पदार्थ विलयन की सतह पर विलेय ठोस तथा विलायक द्रव दोनों के कण उपस्थित होते है, परंतु इसमें से विलायक के कण ही वाष्प में परिवर्तित होते है। इस कारण सतह पर वाष्पित होने वाले कणों की संख्या विलयन में, शुद्ध विलायक की तुलना में कम हो जाती है, जिस कारण विलयन का वाष्पदाब शुद्ध विलायक की तुलना में कम होता है।
Raoult’s Law for Solid-Liquid Solutions.
अवाष्पशील ठोस पदार्थ को किसी विलायक में घोलने पर प्राप्त विलयन का वाष्पदाब केवल विलायक के वाष्पदाब के कारण होता है।
माना ऐसे किसी विलयन में विलायक का वाष्पदाब P1 है व उसका मोलअंश X1 है तथा विलेय की मोलअंश X2 है.
राउल्ट के नियमानुसार,
P1 X1
P1 = P1° X1
Raoult’s law, a special case of Henry’s law.
→ हेनरी के नियमानुसार,
P X
P = KH X -(i)
→ राउल्ट के नियमानुसार,
Pi Xi
Pi = Pi Xi -(ii)
समी. (i) व (ii) की तुलना करने पर हम पाते है कि दोनो समी. में केवल स्थिरांक में भिन्नता है.
हेनरी के नियम के स्थिरांक = KH
राउल्ट के नियम के स्थिरांक = Pi
अत: राउल्ट का नियम हेनरी के नियम की एक विशिष्ट अवस्था है।